氨基酸将不向任一电极移动此时的pH为该氨基酸的等电点,等电点时氨基酸以两性离子存在如RCHNH3+COO的形式等电点是通过实验测出的,根据电离常数也可以计算,但很繁赖氨酸的等电点为974;各种氨基酸在水中的溶解度差别很大,并能溶解于稀酸或稀碱中,但不能溶于有机溶剂通常酒精能把氨基酸从其溶液中沉淀析出 1两性解离与等电点氨基酸在水溶液或结晶内基本上均以兼性离子或偶极离子的形式存在所谓两性。
1两性解离及等电点 氨基酸分子中有游离的氨基和游离的羧基,能与酸或碱类物质结合成盐,故它是一种两性电解质在某一PH的溶液中,氨基酸解离成阳离子和阴离子的趋势及程度相等,成为兼性离子,呈电中性,此时溶液的PH;赖氨酸在等电点的结构式是H2NCH2CH2CH2CH2CHNH2COOH根据相关公开信息显示,含有一个羧基和两个氨基,三个pk表示它的三步电离,最后一步电离才电离完全,达到等电点pi。
在介质pH小于等电点pI时,介质中H+会抑制羧基解离促进氨基解离,使氨基酸主要以阳离子形式存在赖氨酸是人体必需氨基酸之一,能促进人体发育增强免疫功能,并有提高中枢神经组织功能的作用赖氨酸为碱性必需氨基酸;解离方程式HOOCCH2CH2CHNH2 COOH +CH3 CHCH3 CHNH2 COOH +NH2CH2COOH=HOOCCH2HNOCCH2CH2CHNH2 CONHCOOHCHCHCH3 CH3 +2H2O 甘氨酸的解离常数是PK1=234,PK2=960。
在特定的pH值时,氨基酸的正电荷等于负电荷,净电荷为零时,在电场中既不向正极移动,也不向负极移动这时溶液的pH值称为该氨基酸的等电点pI不同氨基酸由于R基团的结构不同而有不同的等电点,范围在277~10。
赖氨酸的两性解离和等电点有关系吗
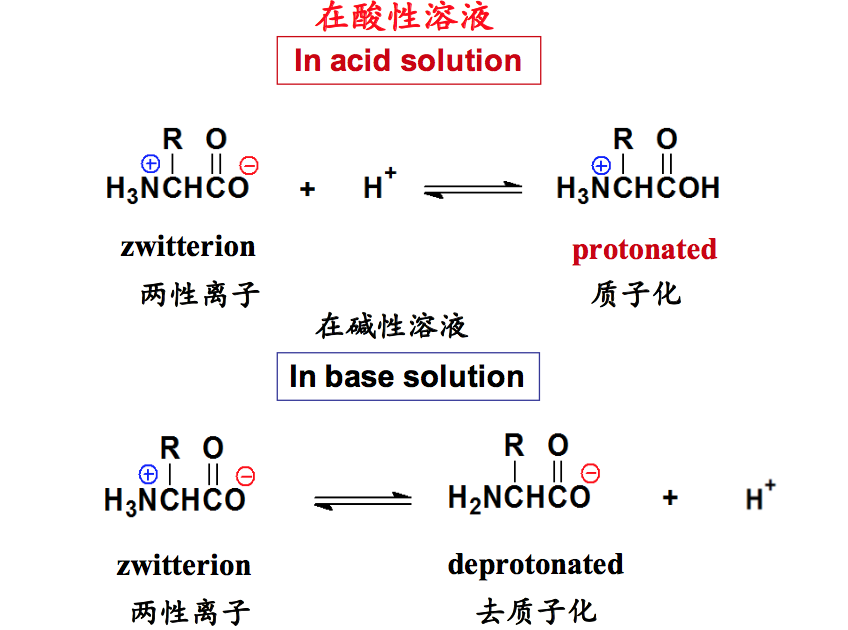
COOα位的氨基上带一个正电荷即NH3+赖氨酸溶液为酸碱两性溶液,其羧酸根可以接受一个氢离子表现为碱性,NH3+也可以给出一个氢离子表现为酸性所以,赖氨酸的解离平衡的书写应分成碱性解离和酸性平衡写。
赖氨酸在水溶液的等电点是974其它氨基酸的等电点甘氨酸597,丙氨酸600,缬氨酸596,亮氨酸598,异亮氨酸602,苯丙氨酸548,丝氨酸568,苏氨酸616,酪氨酸568,半胱氨酸505,蛋氨酸574,脯氨酸6。
等电点最高的氨基酸是赖氨酸其等电点为pH1076,比其他氨基酸如丙氨酸谷氨酸等高赖氨酸是一种必需氨基酸,对于人体的生长发育和蛋白质合成都有重要的作用此外,赖氨酸还参与体内的多种代谢反应,如糖分解和葡萄糖。
ka3是兼性离子形式和一价阴离子形式之间的平衡常数在等电点附近时,主要以一价阳离子和一价阴离子形式存在,二价阳离子形式存在的极少就是说ka1的影响极小,可以忽略谢谢。
因此,氨基酸分子的整体与溶液的ph有关,改变溶液ph可以使氨基酸带上正电荷,负电荷或者正好处于净电荷为零的兼性离子状态,这个ph就是该氨基酸的等电点解离常数pk是水溶液中具有一定离解度的溶质的的极性参数离解。
谷氨酸是酸性氨基酸,等电点322小于7,在中性溶液中主要以负离子形式存在赖氨酸是碱性氨基酸,等电点974大于7,主要是以正离子的形式存在蛋白质是两性电解质,当溶液PH在其等电点以上时蛋白质分子带负电荷。
如磺酸基-SO3H,容易在溶液中离解出H+,故呈强酸性树脂离解后,本体所含的负电基团,如SO3-,能吸附结合溶液中的其他阳离子赖氨酸带正电,被其吸附,谷氨酸带负电,相互排斥,则随洗脱液先流出。
Lys赖氨酸为带电性碱性氨基酸,所以它的等电点为两个大的解离常数之和除以2 所以其等电点PI=105+902=975。
赖氨酸的两性解离和等电点的关系
等电点是总电荷为零的状态,那么就不应该按单个赖氨酸来计算,而是应该将3个放在一起,就是说一个氨基,一个羧基,加上3个赖氨酸侧链总电荷为零因为lys是碱性AA,在等电点状态下,氨基不带电,羧基带一个负电荷,那。
带正电 赖氨酸是碱性氨基酸,等电点大于7,在等电点条件下赖氨酸呈电中性,而中性PHPH=7条件可看成是在赖氨酸等电点条件下加酸由于赖氨酸中NH2可以结合H+,所以加酸后赖氨酸带正电。